先端醫療 | 腫瘤切除手術的黑科技:熒光分子探針
腫瘤切除手術中,往往會因為過度切除而傷害周圍組織或由于切除不徹底而影響病人預后。為了降低復發率和改善患者術后生存質量,腫瘤的精準切除已成為手術的趨勢,而術中引導對外科醫生來說變得至關重要。
目前,外科醫生在術中主要依賴視覺和觸覺反饋。X射線、PET/CT或MRI等成像方式,主要用于術前診斷、手術計劃或中期評估,但他們卻很難整合至手術室場景中。雖然已經有不少醫院開始裝備術中影像設備,但由于成本高以及實際操作復雜而推進緩慢。
熒光引導手術
為了破解技術瓶頸,實現更精準的腫瘤切除,一種叫做“熒光引導手術“(fluorescenceguidedsurgery,FGS)的術中導航技術逐漸成為外科醫生的“寵兒”。該技術利用特定波長激發光照射,激發腫瘤自身熒光、滯留的熒光分子或細胞攝取的外源性熒光物質發出熒光,引導術者對腫瘤進行精準切除。
熒光引導手術多采用近紅外熒光(NIR,700-900nm),如ICG、Cy5和 IRDye800CW等。與可見光相比,NIR熒光組織穿透性好(5-10mm)、散射小、背景熒光低,更適合臨床在體成像。目前,吲哚菁綠(ICG)已作為目前唯一一個被批準用于臨床的NIR熒光已在肝癌顯影和前哨淋巴結顯影等應用上已初見成效。但由于ICG本身并不具有腫瘤靶向性,自此,具有靶向性的熒光分子探針開始進入人們的視野。
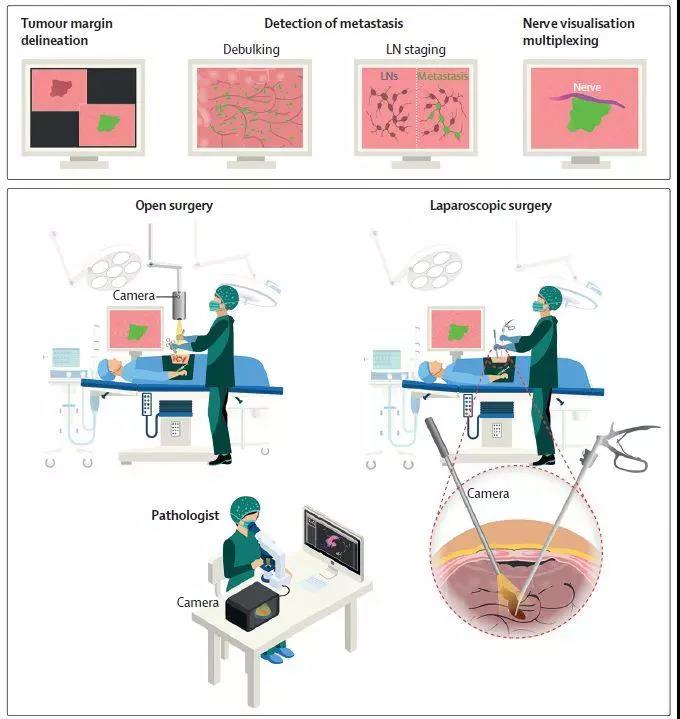
術中熒光分子探針成像原理
上圖:靶向熒光分子探針的潛在應用示意圖。
下圖:在開放和腹腔鏡手術中實施熒光引導。經靜脈注射后的示蹤劑(手術前1小時以內,視示蹤劑而定)、腫瘤或其他目標組織使用專業的近紅外攝像機,從而指導外科醫生實時切除。立即切除后,標本可以在手術室內的后桌(用來分析的桌子)上成像用熒光照相機和顯微鏡觀察組織樣本。因此,病理學家可以快速檢查切除邊緣上的熒光,并提供快速反饋給外科醫生。
靶向熒光分子探針
靶向熒光探針通常由三部分組成:識別基團(recognitionelement)、報告基團(fluorophore)和連接體(linker)。識別基團決定了探針的選擇性和特異性,報告基團決定了其靈敏度,而連接體則可以調節探針的大小、藥代動力學、生物分布和帶電情況等特性。
識別基團是探針最核心的部分,主要有兩種識別策略:一是利用癌細胞表面過表達的受體,如葉酸受體和EGFR等;二是利用腫瘤組織中過表達的酶,如組織蛋白酶(cathepesins)和基質金屬蛋白酶(MMPs)等,這些酶往往和腫瘤的擴散和轉移有關。
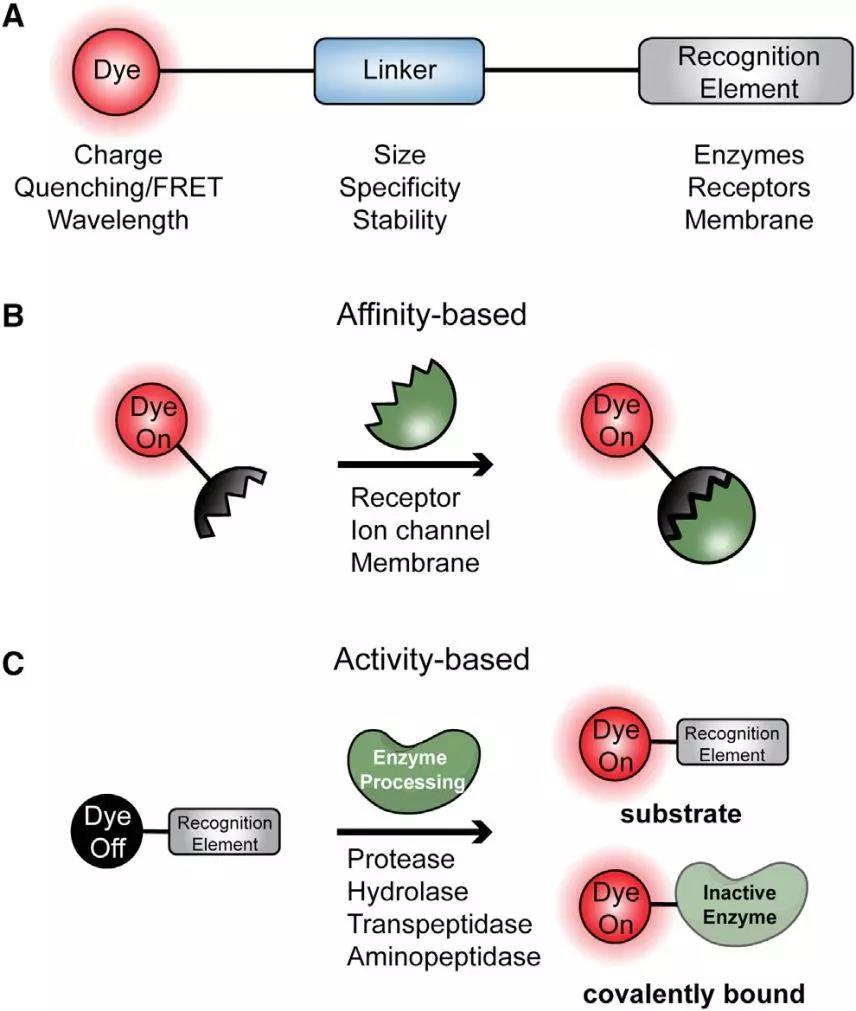
A:探針結構
B:基于配受體結合的探針
C:基于酶激活的探針
靶向熒光分子探針的應用
熒光分子影像借助分子探針和熒光內鏡設備,將肉眼不可見的腫瘤“精準點亮”,廣泛應用于手術導航和早期診斷。
手術導航
手術殘留和預后不良以及癌癥復發息息相關,而過度切除則可能傷害周圍正常組織。因此判斷腫瘤邊界十分重要。靶向熒光探針能夠在術中實時點亮癌細胞,幫助醫生判斷腫瘤邊界和發現轉移灶,這一概念也就是上文提到的熒光引導手術。
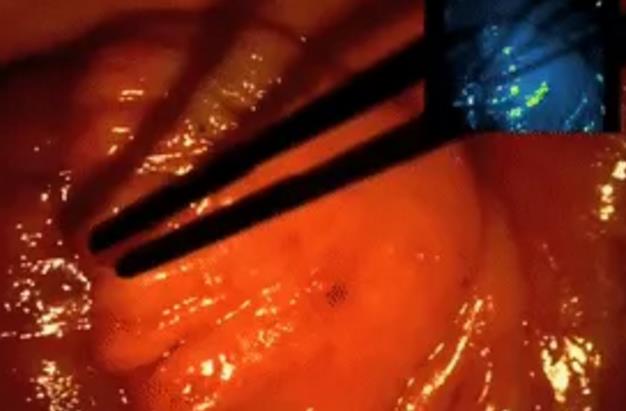
世界首例熒光導航卵巢癌切除術
早期診斷
在我國,消化道惡性腫瘤的發病率和死亡率遠高于世界平均水平。早期消化道癌癥其實并不可怕,預后良好,治療后5 年的生存率高達90%。內鏡是消化道早癌診斷的主要工具,但現有的內鏡檢查技術并不能滿足胃腸癌診斷的臨床需要,早癌診斷率不足20%。
靶向熒光探針可特異性點亮病變細胞,幫助醫生發現容易疏漏的病變,提高早癌的檢出率。
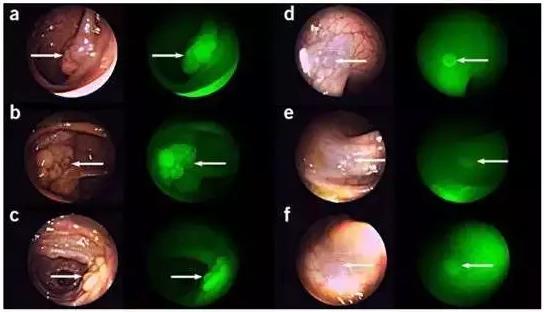
EMI-137探針可提高結直腸病變的檢出率
熒光探針臨床研究的現狀
目前,靶向熒光分子探針的研究國外明顯領先于國內,其中BLZ-100、OTL38、EMI-137和貝伐單抗-IRDye800CW等靶向熒光探針已進入臨床研究,其中OTL38 針對卵巢癌的臨床試驗已進入III期,此外還有一系列探針正在臨床前開發中。


